- Автор Alex Aldridge aldridge@what-difference.com.
- Public 2023-12-17 13:30.
- Последно модифициран 2025-06-01 07:36.
Ключова разлика - алифатни срещу ароматни въглеводороди
Нека първо видим накратко какви въглеводороди обсъждат разликата между алифатни и ароматни въглеводороди. Въглеводородите са органични съединения, съдържащи въглеродни и водородни атоми в структурата си. Ключовата разлика между алифатните и ароматните въглеводороди е, че алифатните въглеводороди не съдържат спрегната система от връзки, докато ароматните въглеводороди съдържат спрегната система на връзки. И двете молекули обаче се считат за органични съединения.
Какво представляват алифатните въглеводороди?
Алифатните въглеводороди са органични молекули, съдържащи въглеродни (C) и водородни (H) атоми в тяхната структура; в прави вериги, разклонени вериги или неароматни пръстени. Алифатните въглеводороди могат да бъдат категоризирани в три основни групи; алкани, алкени и алкини.
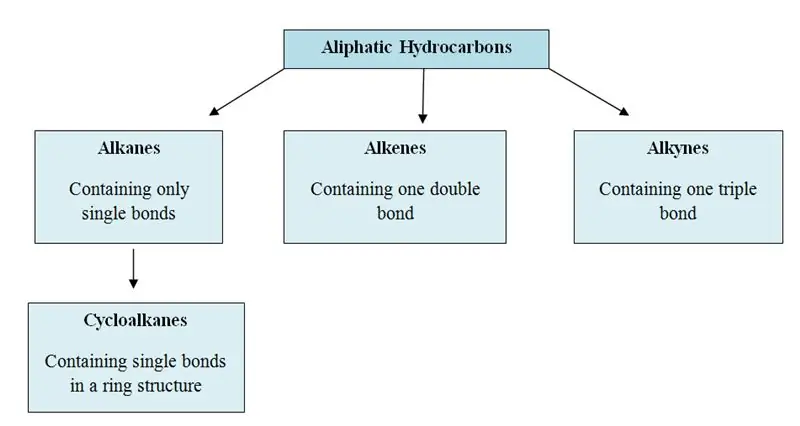
Какво представляват ароматните въглеводороди?
Ароматните въглеводороди понякога са известни като „арени“или „арилови въглеводороди“. Повечето ароматни въглеводороди съдържат бензенов пръстен в тяхната структура; но има небензенови ароматни въглеводороди, наречени хетероарени, които следват „правилото на Хъкъл“(цикличните пръстени, които следват правилото на Хъкъл, имат 4n+2 броя π-електрони; където n=0, 1, 2, 3, 4, 5, 6). Някои ароматни въглеводороди имат повече от един пръстен; те се наричат полициклични ароматни въглеводороди.
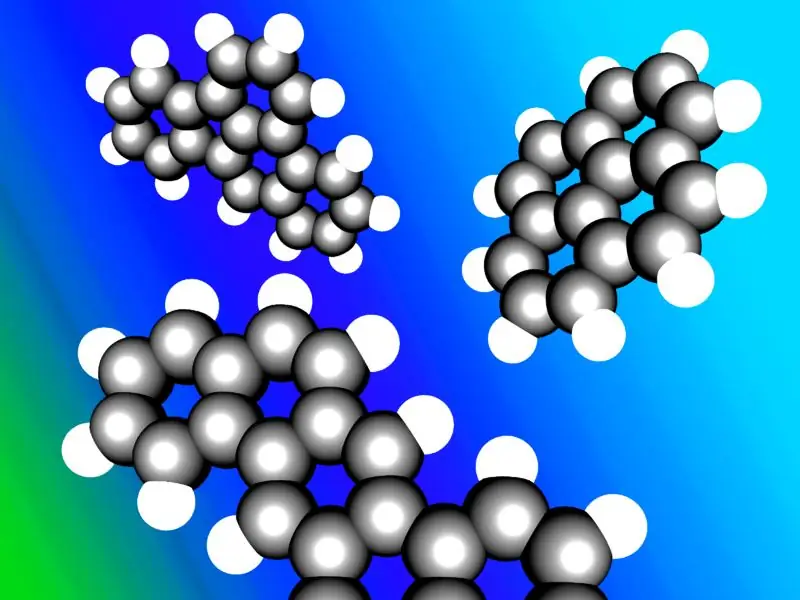
Илюстрация на типични полициклични ароматни въглеводороди.
Каква е разликата между алифатни и ароматни въглеводороди?
Структура на алифатни и ароматни въглеводороди
Алифатни въглеводороди: Те имат прави вериги, разклонени вериги или неароматни пръстени в тяхната структура. Тази група включва както наситени, така и ненаситени въглеводороди. Алканите са наситени въглеводороди, алкените и алкините са ненаситени въглеводороди.
Прави вериги:
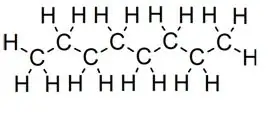
Октан
Маркови вериги:
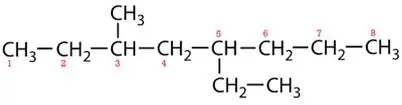
5-етил-3-метилоктан

2-метил-3-пентен
Неароматни пръстени:
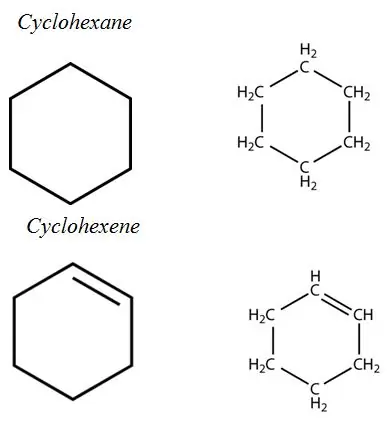
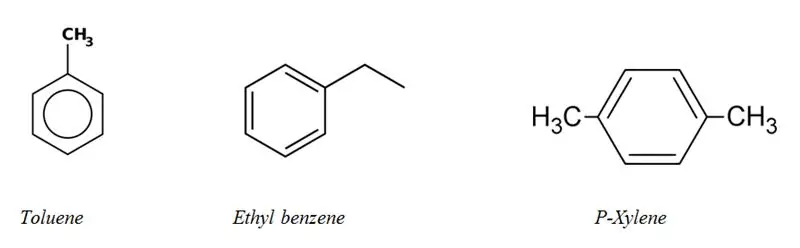
Ароматни въглеводороди: Ароматните въглеводороди имат ароматна пръстенна система в своята структура. Всички те са ненаситени въглеводороди, но относително стабилни поради системата от спрегнати връзки.
Категории алифатни и ароматни въглеводороди
Алифатни въглеводороди:
Има три основни групи в алифатните въглеводороди; алкани, алкени и алкини. Те са известни също като алил въглеводороди.
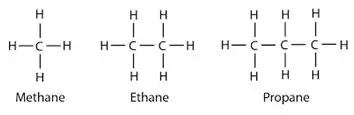
Алкани: В алканите въглеродните и водородните атоми са свързани заедно чрез единични връзки. Те нямат множествени връзки. Алканите образуват пръстенни структури, те се наричат циклоалкани.
Алкени: Тази група съдържа както единични, така и двойни връзки между въглеродните атоми. Водородните и въглеродните атоми винаги образуват единични връзки.
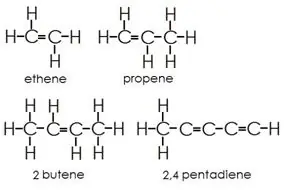
Алкини: Алкините имат тройни връзки между въглеродните атоми в допълнение към единичните връзки.
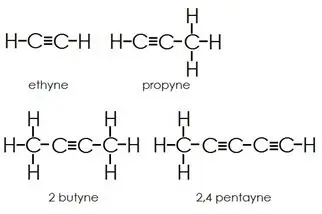
Ароматни въглеводороди:
Повечето от ароматните въглеводороди съдържат поне един бензенов пръстен в структурата си. Но има малко небензенови ароматни въглеводороди, те се наричат "хетероарени". Ароматните въглеводороди се наричат "арилни" въглеводороди.
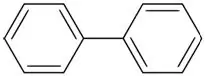
Бифенил (ароматен въглеводород с два бензенови пръстена)
Модел на свързване на алифатни и ароматни въглеводороди
Алифатни въглеводороди:
В алифатни въглеводороди; единични, двойни или тройни връзки могат да съществуват навсякъде в молекулата. Понякога може да има няколко структури за една молекулна формула чрез промяна на позицията на множествената връзка(и). Тези молекули имат локализирана електронна система.
Ароматни въглеводороди:
В ароматните въглеводороди те имат алтернативна система от единични и двойни връзки, за да образуват система от спрегнати връзки за делокализиране на някои електрони. (Делокализираните електрони могат да се преместват от една връзка в друга).
Реакции на алифатни и ароматни въглеводороди
Алифатни въглеводороди:
Наситените въглеводороди претърпяват реакции на заместване; ненаситените въглеводороди постигат стабилност чрез реакция на присъединяване. Но някои реакции протичат при контролирани условия, без да се разрушават множество връзки.
Ароматни въглеводороди:
Ароматните въглеводороди са ненаситени, но имат стабилна система от спрегнати електрони, така че са по-податливи на реакции на заместване, отколкото на реакции на добавяне.
Изображението е предоставено с любезно съдействие: „Полициклични ароматни въглеводороди“от Inductiveload - Собствена работа от качващия, Accelrys DS Visualizer. (Обществено достояние) чрез Commons






